- Una pila de combustible convierte de forma directa energía química en electricidad mediante reacciones electroquímicas sin combustión.
- El sistema completo integra el stack con subsistemas de combustible, oxidante, refrigeración, seguridad y electrónica de potencia.
- Existen varios tipos principales (PEM, DMFC, AFC, PAFC, MCFC, SOFC) adaptados a distintos rangos de temperatura y aplicaciones.
- Las pilas de combustible ya se usan en cogeneración, transporte, logística y aplicaciones críticas, con eficiencias eléctricas del 40–60 % y aún amplias posibilidades de mejora.
Las pilas de combustible han pasado de ser una curiosidad de laboratorio en el siglo XIX a convertirse en una de las tecnologías clave de la transición energética. A día de hoy están presentes en aplicaciones tan diversas como naves espaciales, edificios, vehículos, instalaciones industriales o montacargas de almacén, y se consideran una de las piezas centrales de la llamada economía del hidrógeno.
Pese a que últimamente se habla mucho de ellas, la realidad es que su historia es larga y compleja, y su funcionamiento tiene bastante más miga de lo que suele contarse en folletos divulgativos. En las siguientes líneas vamos a recorrer con detalle qué es un sistema de pila de combustible, cómo se estructura, qué tipos existen, qué rendimiento alcanzan y en qué aplicaciones reales ya se están usando, apoyándonos en la experiencia acumulada por la industria y por la investigación académica.
Breve recorrido histórico de las pilas de combustible
La historia de las pilas de combustible arranca mucho antes de lo que suele pensarse. A finales de la década de 1830, el científico suizo Christian Friedrich Schönbein y el galés William Robert Grove estudiaron las llamadas baterías gaseosas basadas en hidrógeno y oxígeno. Grove presentó en 1843 su dispositivo «Gas Voltaic Battery», donde conectó eléctricamente cincuenta celdas con electrodos de platino en ácido sulfúrico alimentados con H2 y O2, logrando incluso invertir la electrólisis del agua.
En ese montaje, la reducción de oxígeno tenía lugar en el cátodo, combinándose con iones H+ para dar agua, mientras que en el ánodo se oxidaba el hidrógeno generando los electrones que circulaban por el circuito externo. A partir de ahí, figuras como Lord Rayleigh mejoraron el diseño aumentando la superficie de contacto entre electrodos, gases y electrolito, lo que incrementó notablemente la eficiencia del sistema.
En 1889, Ludwig Mond y Charles Langer acuñaron el término «pila de combustible» y propusieron un diseño en el que el electrolito se retenía en una matriz sólida porosa recubierta de una fina capa de platino u oro. Esta configuración resolvía el problema de accesibilidad de los gases a la zona activa de los electrodos, un cuello de botella clave en los primeros dispositivos.
El siguiente gran salto llegó en 1954, cuando Francis Thomas Bacon construyó una planta de 5 kW con una pila alcalina de hidrógeno y oxígeno usando ánodo de níquel, cátodo de óxido de níquel-litio e hidróxido potásico concentrado como electrolito. Este sistema demostró por primera vez potencias útiles continuas, hasta el punto de emplearse en los años 60, bajo licencias de Pratt & Whitney, en las misiones espaciales estadounidenses para generar electricidad y agua potable a bordo.
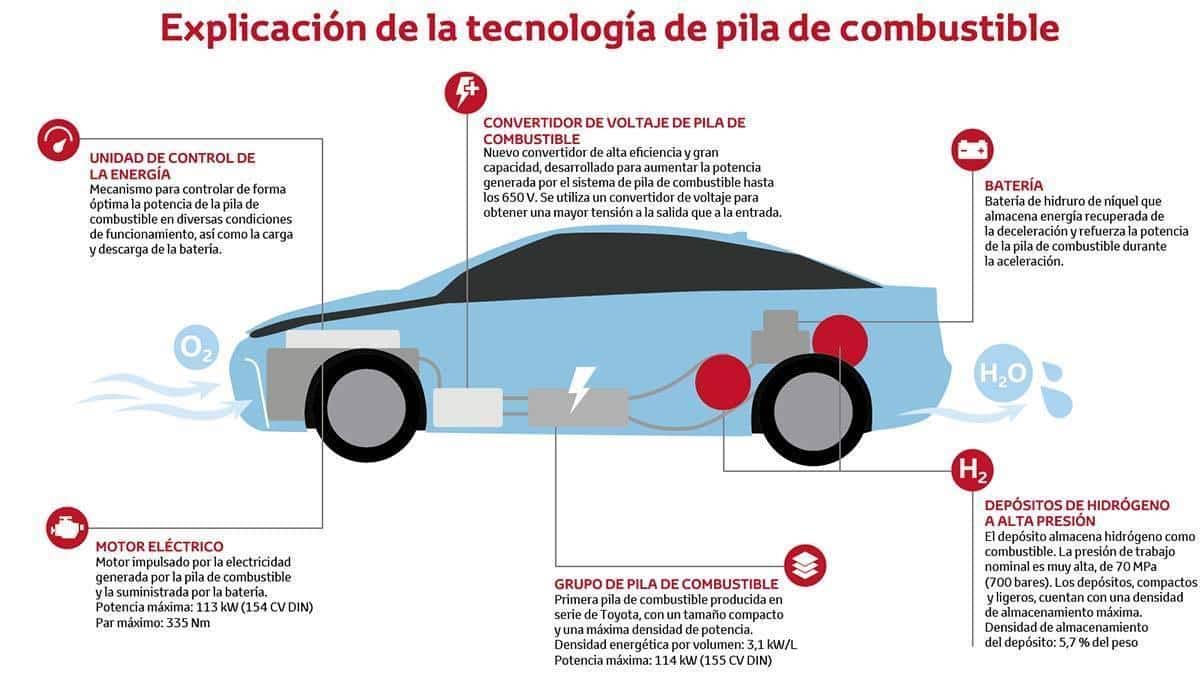
En paralelo, General Electric desarrolló para el programa Gemini las primeras pilas de membrana de intercambio de protones (PEMFC), tecnología que más tarde se convertiría en el caballo de batalla de la automoción, como demuestra el compromiso de Toyota con el hidrógeno en la movilidad sostenible.
Qué es exactamente una pila de combustible y en qué se diferencia de una batería
Una pila de combustible es, en esencia, un dispositivo electroquímico que convierte energía química directamente en electricidad mediante reacciones de oxidación-reducción. Usa un combustible (habitualmente hidrógeno) y un oxidante (casi siempre oxígeno o aire) que se alimentan de forma continua a la celda.
A diferencia de una batería convencional, cuyos reactivos están almacenados en su interior y se agotan, la pila de combustible no se descarga en el sentido clásico: seguirá produciendo electricidad mientras se mantenga el suministro de combustible y oxidante desde el exterior. En términos prácticos, es más parecido a un generador electroquímico continuo que a un acumulador.
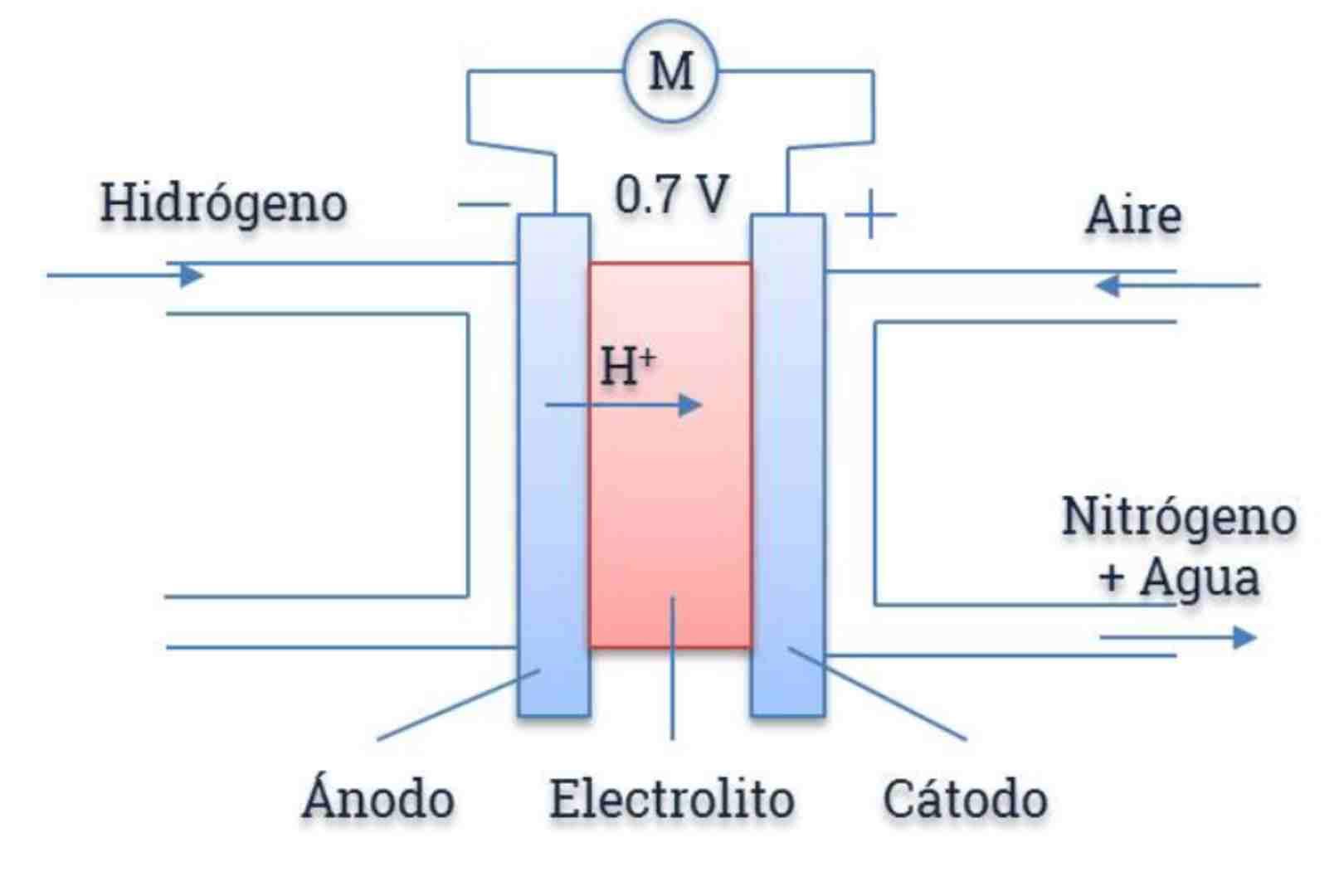
De forma muy esquemática, una celda unitaria consta de un ánodo (electrodo negativo), un cátodo (electrodo positivo) y un electrolito situado entre ambos. El electrolito sólo permite el paso de iones, bloqueando el de electrones. Estos, al no poder cruzar por el electrolito, se ven obligados a circular por el circuito externo, generando la corriente útil.
Cuando el combustible se oxida en el ánodo se liberan iones y electrones; los iones viajan a través del electrolito hacia el cátodo, donde el oxidante se reduce captando esos electrones que han recorrido el circuito externo. Este sencillo esquema se complica al pasar de una única celda a un apilamiento (stack) de muchas celdas conectadas en serie, que es como se obtienen tensiones y potencias útiles en la práctica.
Elementos básicos de una celda de combustible
En una celda típica (por ejemplo, de tipo PEM) encontramos los siguientes componentes esenciales, que luego se replican en un apilamiento:
Electrolito: es el medio que conduce iones (protones en una PEM, iones hidroxilo en una AFC, carbonatos, oxígeno, etc.) pero actúa como aislante electrónico. Puede ser líquido (ácidos o bases en solución) o sólido (membranas poliméricas o cerámicas). Su misión es triple: permitir el paso selectivo de iones, separar físicamente ánodo y cátodo y evitar el cruce directo de gases, que cortocircuitaría la celda.
Electrodos: normalmente porosos para facilitar la difusión de los gases, son las superficies donde tienen lugar las reacciones electroquímicas. En el ánodo se oxida el combustible y en el cátodo se reduce el oxidante. Su estructura multicapa garantiza el contacto entre las tres fases involucradas: sólido (electrodo+catalizador), gaseosa (reactivos) y líquido o sólido (electrolito).
Los electrodos deben asegurar una buena conductividad eléctrica para evacuar o aportar electrones, distribuir homogéneamente los gases sobre el área activa y permitir la retirada eficiente de los productos (agua, CO2, etc.), evitando inundaciones o zonas secas.
Placas bipolares: en los apilamientos, estas placas separan celdas adyacentes, canalizan la distribución de gases (mediante canalizaciones grabadas o mecanizadas) y conducen la corriente entre celdas. Suelen fabricarse en grafito, aceros especiales o compuestos conductores, y deben combinar baja resistencia eléctrica, resistencia a la corrosión y buena rigidez mecánica.
Al combinar muchas celdas (típicamente más de 45 en aplicaciones automotrices) se obtiene un «fuel cell stack» con tensiones de salida y densidades de potencia aptas para aplicaciones reales. A su alrededor se organiza el llamado balance de planta o BOP, que agrupa todos los subsistemas auxiliares.
Del stack al sistema completo de pila de combustible
Una cosa es la celda (o el apilamiento) y otra el sistema de pila de combustible completo. Este último incluye todos los elementos necesarios para que el stack funcione de forma segura, fiable y con parámetros controlados en una aplicación concreta (vehículo, edificio, planta de generación, montacargas, etc.).
Los subsistemas más habituales dentro de un sistema de pila de combustible de hidrógeno son:
Sistema de suministro de combustible: abarca el tanque o tanques de almacenamiento (a alta presión, criogénicos o de hidruros metálicos), las válvulas, reguladores de presión, eventuales bombas o compresores y, en su caso, reformadores externos cuando el combustible de entrada no es hidrógeno puro (gas natural, metanol, etanol, biogás, etc.).
Sistema de suministro de oxidante: típicamente aire comprimido o, en aplicaciones especiales, oxígeno puro. Incluye compresores o soplantes, filtros, sistemas de deshumidificación y, en algunos diseños, etapas de purificación de CO2 o contaminantes para evitar el envenenamiento del cátodo.
Sistema de refrigeración: al tratarse de reacciones exotérmicas, el stack genera calor que debe evacuarse. Según el tipo de pila y su temperatura de operación, se recurre a circuitos de refrigeración por agua, glicoles o aire forzado, con bombas, intercambiadores de calor y, a menudo, integración con sistemas de climatización o cogeneración.
Sistema eléctrico y de acondicionamiento de potencia: la pila genera corriente continua con un perfil de tensión variable en función de la carga. Para poder integrarla en una red, en una batería o en la electrónica de un vehículo se emplean convertidores DC/DC, inversores DC/AC, sistemas de protección y gestión de energía que adaptan la salida del stack a las necesidades de la carga.
Además de estos bloques principales, un sistema moderno incluye sensores, controladores electrónicos, sistemas de seguridad (detección de fugas de gas, válvulas de alivio, enclavamientos, etc.) y, cuando procede, módulos de almacenamiento energético adicionales (baterías o supercondensadores) para gestionar picos de potencia y recuperación de energía.
Principios electroquímicos y rendimiento termodinámico
Desde el punto de vista termodinámico, la máxima cantidad de trabajo eléctrico que puede extraerse de una pila de combustible en condiciones reversibles viene dada por la variación de energía libre de Gibbs de la reacción global. Para la reacción clásica hidrógeno-oxígeno:
H2 + 1/2 O2 → H2O
en condiciones estándar (298,15 K y 1 atm), la entalpía de reacción es aproximadamente 285,8 kJ/mol y la energía libre de Gibbs unos 237,1 kJ/mol. El rendimiento ideal teórico, definido como ΔG/ΔH, ronda el 83 % para esta reacción, muy por encima de los límites impuestos por el ciclo de Carnot en máquinas térmicas convencionales.
El potencial eléctrico máximo (en circuito abierto) se obtiene a partir de la ecuación de Nernst, que relaciona el potencial de celda con las actividades (o presiones parciales) de reactivos y productos. En una pila de hidrógeno y oxígeno, el potencial estándar es algo superior a 1,2 V por celda, aunque en la práctica la tensión en carga se sitúa alrededor de 0,7 V por celda debido a diversas pérdidas.
La eficiencia real se define como el cociente entre el trabajo eléctrico realmente obtenido y la energía química suministrada. Suele expresarse, de manera práctica, como el producto del rendimiento ideal por el cociente entre el voltaje real bajo carga y el voltaje ideal en circuito abierto. A esto hay que añadir, si se quiere ser preciso, el factor de aprovechamiento del combustible, ya que raramente se utiliza el 100 % del reactivo alimentado.
En sistemas bien diseñados, las pilas de combustible pueden alcanzar rendimientos eléctricos del orden del 40-60 %. En configuraciones de cogeneración (aprovechando además el calor residual), la eficiencia global puede acercarse al 80-90 % en aplicaciones estacionarias, valores difíciles de igualar por tecnologías basadas en combustión.
Pérdidas y curva de polarización: activación, ohmia y concentración
Cuando por la pila circula corriente aparecen una serie de fenómenos que provocan que la tensión de salida sea menor que el potencial de Nernst. Estos fenómenos se visualizan en la llamada curva de polarización, que representa el voltaje de la celda frente a la densidad de corriente.
En la zona de bajas corrientes predominan las pérdidas por activación, asociadas a la energía de activación de las reacciones electroquímicas. Se describen mediante ecuaciones tipo Tafel, donde la caída de potencial depende logarítmicamente de la densidad de corriente e inversamente de la temperatura, del número de electrones transferidos y del coeficiente de transferencia de carga.
En una zona intermedia se imponen las pérdidas óhmicas, ligadas a la resistencia al paso de electrones a través de los electrodos y de iones a través del electrolito, así como a las resistencias de contacto. En este régimen, la caída de tensión aumenta aproximadamente de forma lineal con la corriente (clásica ley de Ohm).
A altas densidades de corriente aparece la región de polarización por concentración. El transporte de masa (difusión de reactivos hacia las superficies activas y retirada de productos) se vuelve limitante, se generan gradientes de concentración y, por tanto, una caída adicional de potencial. Una idea clave es la corriente límite, que refleja la máxima velocidad a la que los reactivos pueden suministrarse al electrodo.
Mitigar estas pérdidas pasa por combinar estrategias como: uso de catalizadores más activos, incremento moderado de la presión y temperatura de operación, diseño de canales de flujo y porosidad de electrodos que optimicen la difusión de gases, utilización de membranas más conductoras y delgadas, y una correcta gestión del agua (especialmente crítica en PEMFC).
Gestión del agua, temperatura y flujo en pilas PEM
En las pilas de membrana de intercambio protónico (PEMFC) la membrana polimérica debe mantenerse adecuadamente hidratada. Su conductividad protónica depende fuertemente del contenido de agua: si se seca aumenta la resistencia interna, se agrieta y pueden aparecer cortocircuitos de gas; si se inunda, los electrodos se bloquean y los reactivos no alcanzan el catalizador.
Por ello, resulta esencial controlar con precisión la humidificación de los gases de entrada, el diseño de los canales de flujo y el sistema de evacuación del agua producida en el cátodo. Una de las líneas de investigación más activas se centra precisamente en optimizar la gestión del agua para ampliar la ventana operativa de estas pilas.
La temperatura también debe ser lo más uniforme posible en todo el apilamiento para evitar tensiones térmicas y degradación prematura de materiales. En sistemas de potencia media y alta se recurre a elaborados circuitos de refrigeración integrados en las placas bipolares o en estructuras adyacentes.
El control del flujo de combustible y oxidante es igualmente crítico. Al igual que en un motor de combustión se echa mano de relaciones estequiométricas óptimas, en una pila de combustible hay que asegurar una relación constante entre caudal de reactivos y corriente demandada para maximizar la eficiencia y minimizar zonas muertas o con exceso de combustible.
Tipos principales de pilas de combustible
La clasificación más extendida de las pilas de combustible se basa en el tipo de electrolito, lo que a su vez determina los iones que se transportan, la temperatura de operación y, en buena medida, las aplicaciones idóneas.
PEMFC (Proton Exchange Membrane Fuel Cell): utilizan una membrana polimérica sólida (como Nafion o alternativas más económicas) que conduce protones. Trabajan típicamente entre 80-95 ºC, con eficiencias eléctricas de 40-60 % a nivel de pila y algo menores a nivel de sistema. Ofrecen alta densidad de potencia, arranque rápido y buena respuesta dinámica, por lo que son las favoritas para automoción, aplicaciones portátiles y sistemas de respaldo.
HT-PEM (PEM de alta temperatura): una variante que emplea membranas capaces de operar entre 120 y 200 ºC, lo que mejora la tolerancia a impurezas (como el CO), facilita el uso de reformadores integrados y simplifica la gestión de agua, a costa de requisitos más exigentes en materiales y sellados.
DMFC (Direct Methanol Fuel Cell): también usan membrana polimérica, pero el combustible es metanol líquido, oxidado directamente en el ánodo. Operan en el rango de 50-120 ºC y destacan por la facilidad de transporte y almacenamiento del combustible. Se orientan a dispositivos portátiles, electrónica de consumo y aplicaciones de pequeña potencia, aunque su eficiencia es más baja que la de las PEM de hidrógeno.
AFC (Alkaline Fuel Cell): emplean una disolución acuosa de hidróxido de potasio como electrolito y operan entre 105-245 ºC. Pueden utilizar catalizadores no nobles y alcanzan eficiencias de 60-70 %, pero son muy sensibles al CO2, que degrada el electrolito formando carbonatos. Han sido ampliamente utilizadas por la NASA y en aplicaciones espaciales y submarinas.
PAFC (Phosphoric Acid Fuel Cell): usan ácido fosfórico líquido como electrolito y funcionan a 180-205 ºC. Soportan combustibles reformados con mayor contenido de impurezas y se han consolidado como opción para cogeneración estacionaria en edificios y complejos comerciales, con potencias del orden de cientos de kW.
MCFC (Molten Carbonate Fuel Cell): emplean carbonatos alcalinos fundidos sobre una matriz cerámica, operando alrededor de 650 ºC. Esta alta temperatura permite el reformado interno de hidrocarburos, incluso a partir de gases derivados del carbón, y otorga alta eficiencia y flexibilidad en el combustible, a costa de problemas de corrosión y arranque lento.
SOFC (Solid Oxide Fuel Cell): utilizan electrolitos cerámicos sólidos (como zirconia estabilizada con itria) que conducen iones oxígeno a temperaturas típicas de 800-1000 ºC. Son idóneas para generación estacionaria y cogeneración a gran escala, ofreciendo eficiencias eléctricas de 50-60 % y posibilidad de integración con turbinas de gas para ciclos híbridos de altísima eficiencia global. El reto actual es reducir la temperatura de operación (IT-SOFC) mediante nuevos materiales y capas de electrolito más finas.
Otros tipos de pilas especiales y emergentes
Además de los grandes grupos anteriores, existe una amplia familia de pilas de combustible especializadas: pilas de hidruros metálicos, pilas electro-galvánicas, pilas de ácido fórmico, pilas de borohidruros, pilas de etanol directo, pilas REDOX con electrolitos líquidos, pilas cerámicas protónicas, pilas de carbono, pilas microbianas y bio-pilas enzimáticas, entre otras. Muchas de ellas se encuentran en fase de investigación o nichos de mercado concretos, pero ilustran bien la versatilidad del concepto.
Cada una intenta explotar ventajas concretas (combustibles de fácil manejo, materiales baratos, integración en procesos biológicos, etc.) a costa de desafíos propios en cuanto a densidad de potencia, durabilidad o coste por kW instalado.
Eficiencia global del sistema y comparativa con otras tecnologías
En condiciones de laboratorio, una celda de combustible bien optimizada puede rondar el 50 % de eficiencia eléctrica. Sin embargo, en sistemas reales hay que considerar también las pérdidas ligadas a compresión de gases, gestión térmica, electrónica de potencia, producción y almacenamiento de hidrógeno y demás elementos del balance de planta.
Si se analiza un vehículo de pila de combustible alimentado con hidrógeno comprimido, la eficiencia «pozo a rueda» (desde la producción de hidrógeno hasta la energía mecánica en las ruedas) puede situarse en torno al 20-25 % dependiendo de la ruta de producción del hidrógeno (electrólisis, reformado de gas natural, etc.). En el caso de hidrógeno líquido, las pérdidas asociadas a la licuefacción reducen aún más esta eficiencia global.
En aplicaciones de almacenamiento de energía renovable, el ciclo completo electricidad → hidrógeno (electrólisis) → electricidad (pila de combustible) logra eficiencias redondas del orden del 30-40 %. Pese a no ser espectaculares, estos sistemas tienen la ventaja de poder almacenar grandes cantidades de energía a largo plazo, algo que las baterías cubren peor.
En cogeneración, en cambio, el aprovechamiento del calor residual permite obtener eficiencias globales cercanas al 80 % en sistemas residenciales y comerciales, mientras que en grandes plantas con MCFC o SOFC integradas con turbinas de gas se han reportado eficiencias de sistema superiores al 60 % en electricidad más una fracción adicional en calor útil.
Aplicaciones reales: de la vivienda al submarino
Las pilas de combustible se han consolidado en una gama muy amplio de casos de uso, tanto estacionarios como móviles y portátiles.
En el ámbito estacionario, destacan los sistemas de cogeneración doméstica y para edificios, donde unidades basadas en PAFC, PEMFC o SOFC de pequeña y mediana potencia suministran electricidad de base y calor para calefacción y agua caliente. Países como Japón han liderado su despliegue a través de programas como ENE-FARM.
En el sector industrial y de telecomunicaciones, las pilas de combustible se emplean como fuentes de energía de emergencia y sistemas de alimentación ininterrumpida (UPS), así como para alimentar repetidores, estaciones remotas, centros de datos o infraestructuras críticas que requieren muy alta fiabilidad y poco mantenimiento.
En movilidad, los autobuses de pila de combustible han recorrido ya millones de kilómetros en ciudades de todo el mundo, mostrando menores emisiones locales, reducción del ruido y mejor rendimiento en consumo respecto a autobuses diésel o de gas natural. Los montacargas de almacén equipados con pilas PEM se han popularizado por su capacidad de recarga en pocos minutos, funcionamiento continuo en varios turnos y buen desempeño a baja temperatura, especialmente en cámaras frigoríficas.
En el ámbito marítimo y submarino, varios proyectos han incorporado pilas de combustible como fuente principal o auxiliar de energía. Submarinos avanzados no nucleares emplean sistemas AIP (Air Independent Propulsion) basados en pilas de combustible que les permiten permanecer sumergidos semanas sin emerger, con una firma acústica y térmica muy reducida. También se han desarrollado ferris, barcos de investigación y embarcaciones recreativas propulsados parcial o totalmente por hidrógeno y pilas de combustible.
En aeronáutica y aeroespacio, las pilas de combustible llevan décadas a bordo: desde los programas Gemini y Apolo hasta proyectos más recientes de aviones no tripulados de larga autonomía, auxiliares de potencia a bordo y demostradores de vuelo tripulado alimentados por pilas de hidrógeno. Su bajo nivel de ruido, alta densidad energética del combustible y posibilidad de generar agua a bordo las hace especialmente atractivas para ciertas misiones.
Economía, materiales y retos tecnológicos
En los últimos años la industria de las pilas de combustible ha superado la barrera del milmillón de dólares en facturación anual y el número de apilamientos enviados crece a ritmos elevados. Aun así, el coste por kilovatio sigue siendo un factor crítico para su implantación masiva, sobre todo en automoción y generación distribuida.
Una parte sustancial del coste reside en los catalizadores, tradicionalmente basados en platino. Aunque se han logrado reducciones importantes de carga (por ejemplo, del orden del 30 % en algunos diseños comerciales), se sigue investigando en alternativas con metales no nobles, aleaciones optimizadas y materiales inspirados en enzimas biológicas, como complejos hierro-nitrógeno o estructuras tipo hidrogenasa.
También se trabaja intensamente en nuevas membranas poliméricas más baratas y resistentes, en electrolitos cerámicos con alta conductividad a temperaturas intermedias y en placas bipolares ligeras y con mejor resistencia a la corrosión. La durabilidad es otro frente clave: para ser competitivas en automoción se requieren vidas útiles de al menos 5.000 horas (unos 200.000 km), mientras que en aplicaciones estacionarias se aspira a más de 40.000 horas fiables de operación.
Por último, la infraestructura de hidrógeno (producción, transporte, almacenamiento y red de hidrogeneras) condiciona de forma decisiva el despliegue de vehículos de pila de combustible y de otras aplicaciones basadas en hidrógeno. Países y regiones como la UE, Japón o Corea del Sur han lanzado estrategias nacionales centradas en el hidrógeno verde producido con renovables, básico para que esta tecnología sea realmente climáticamente neutra.
En conjunto, las pilas de combustible y sus sistemas asociados representan una familia tecnológica madura en algunos nichos y aún emergente en otros, con un potencial enorme para aportar electricidad y calor de forma eficiente, flexible y, si se alimentan con combustibles limpios, prácticamente libre de emisiones contaminantes y de gases de efecto invernadero.
